Angepasste Therapien und Biomarker verbessern den Krankheitsverlauf bei MS
Bericht:
Dr. rer. nat. Torsten U. Banisch
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Neue Biomarker und sensitivere Analysemethoden erleichtern die Behandlungsauswahl bei Multipler Sklerose und bilden den Krankheitsverlauf unter den Therapien immer verlässlicher ab. Auf der 22. Jahrestagung der Österreichischen Gesellschaft für Neurologie wurden die neuesten Entwicklungen und die aktualisierten Behandlungsrichtlinien vorgestellt.
Prädiktoren für die Primärtherapie
„Generell sollte unbehandelten Pati-ent:innen mit schubförmig remittierender Multipler Sklerose (RRMS) eine Immuntherapie angeboten werden, wenn ein klinisch objektivierbarer Schub oder eine MRT-Aktivität in einem Zeitraum von2 vorausgegangenen Jahren nachweisbar war“, erklärte Priv.-Doz. Dr. Harald Hegen von der Medizinischen Universität Innsbruck.1 Die vorhandenen Behandlungsalternativen werden in 3 Kategorien mit moderater bis hoher Wirksamkeit unterteilt. Eine Vergleichsstudie konnte zeigen, dass der frühe Einsatz von hocheffektiven Therapien langfristig die Krankheitsprogression verzögern kann.2 Da diese aber Nebenwirkungen verursachen können, sollte jeweils eine individualisierte Therapieentscheidung getroffen werden. Die Therapiewahl wird von einer Reihe von Risikofaktoren unterstützt, beispielsweise demografischen Faktoren, klinischen Aspekten wie Anzahl von Schüben, kompletter Remission der Symptomatik, Grad der Behinderung, möglichen Pyramidenbahnbeteiligung im frühen Krankheitsverlauf, als auch der MRT-Befunde.1–3
Initiierung der Zweitlinientherapie
„Es ist empfehlenswert, unter einer laufenden moderat wirksamen Therapie regelmäßig zu überprüfen, ob auch subklinische Krankheitsaktivität vorliegt und eine Therapieeskalation notwendig ist“, so Hegen. Dies wird nötig, wenn ein erneuter Krankheitsschub auftritt oder, wie neu in den Leitlinien verankert, eine wiederholte MRT-Aktivität oder eine deutliche Zunahme der T2-Läsionslast vorliegt.1 Grundlage für diese Neuerung war eine Studie, die zeigte, dass eine therapeutische Reaktion auf vermehrte Läsionen einen klinisch signifikanten Vorteil brachte.4
Wahl der Therapie
Bei der Therapiewahl gibt es innerhalb der Kategorie 1 (u.a. Dimethylfumarat, Teriflunomid, Injectables) kaum Unterschiede in der Wirksamkeit. So kann die Auswahl anhand von Patient:innen-präferenz und unter Berücksichtigung von Nebenwirkungsprofilen und Komorbiditäten erfolgen.
Bei den hocheffektiven Substanzen (Kategorie 2 und 3), wie den Anti-CD20-Antikörpern (u.a. Ocrelizumab, Ofatumumab, Ublituximab) oder Natalizumab, kann eine Risikostratifizierung hinsichtlich der progressiven multifokalen Leukenzephalopathie (PML) mittels Anti-John-Cunningham-Virus(JCV)-Antikörper-Index für die Behandlungswahl aufschlussreich sein. So sollte bei JCV-Positivität keine Therapie mit Natalizumab erfolgen.1,5 Da circa 70% der Betroffenen weiblich sind, ist auch die Familienplanung bei der Wahl der Immuntherapie zu berücksichtigen. Kontraindiziert sind in diesem Zusammenhang Behandlungen mit Teriflunomid, S1P und Alemtuzumab.
Limitierte Therapieoptionen bei sekundär progredienter MS
Bei der sekundär progredienten MS (SPMS) liegt eine schubunabhängige Behinderungsprogression vor. Zur Therapieentscheidung sollte eine Klassifizierung in aktive SPMS (zusätzliche Schübe, MRT-Aktivität) oder nicht aktive SPMS erfolgen. Nach der aktuellen Studienlage stehen bisher nur für die aktive SPMS wirksame Immuntherapeutika, wie Siponimod, Cladribin, Ponesimod und Anti-CD20-Antikörper zur Verfügung. Ein junges Lebensalter, eine kurze Krankheitsdauer und ein geringer Behinderungsgrad sind hier Prädiktoren für einen therapeutischen Nutzen.
Anti-CD20-Antikörper als einzige Therapieoption bei primär progredienter MS
15% der MS-Patient:innen haben eine primär progrediente Erkrankung (PPMS). Hier steht mit den Anti-CD20 Antikörpern bisher nur eine Substanzklasse für die Behandlung zur Verfügung. Nach der aktuellen Studienlage kann Ocrelizumab eingesetzt werden. Bei Patient:innen jenseits des 50. Lebensjahres und insbesondere beim Fehlen von entzündlicher MRT-Aktivität sollte die Indikation für Ocrelizumab streng gestellt werden. Im individuellen Fall kann jedoch bei rascher Zunahme der Behinderung mit drohendem Verlust der Selbstständigkeit ein Therapieversuch zunächst begrenzt auf 2 Jahre erwogen werden, da Therapiealternativen fehlen.1
Update: Monitoring und Evaluation des Therapieerfolgs
„Bei der MS-Behandlung spielen gerade das Monitoring und die Evaluation des Therapieerfolgs für eine zeitnahe Anpassung oder Therapieeskalation eine zentrale Rolle“, erklärt Assoz. Prof. Priv.-Doz. Dr. Michael Khalil von der Medizinischen Universität Graz. Zu den Prädiktoren für eine schlechte Prognose zählen neben demografischen und klinischen Faktoren auch die Biomarker. Hierunter fallen die Anzahl von T2-Läsionen, das Vorhandensein von oligoklonalen IgG- und IgM-Banden im Liquor, hohe Konzentrationen von Chitinasen im Liquor oder eine mittels optischer Kohärenztomografie nachgewiesene Ausdünnung der retinalen Nervenfeuerschicht. Immer öfter werden auch die Konzentrationen der Neurofilamentleichtketten im Liquor und Serum für die Beurteilung herangezogen.6
Aktuelle und künftige Rolle des MRT in der Verlaufskontrolle
MRT in der Verlaufskontrolle mit T1- oder T2-Gewichtung identifizieren Läsionen und Gewebeschäden. Durch die „double inversion recovery“ können schwierig darzustellende kortikale Läsionen erkannt werden. Eine weitere optionale Methode ist das „magnetization transfer imaging“, das strukturelle Schädigungen im Hirn quantifizieren kann.7
Generell sollte anfänglich immer eine MRT-Baseline-Untersuchung erfolgen und eine neue Baseline 3–6 Monate nach Behandlungsbeginn erstellt werden. Bei den meisten Patient:innen genügt anschließend ein jährliches Kontroll-MRT. Hier wird überprüft, ob sich neue, vergrößernde oder Kontrastmittel aufnehmende Läsionen gebildet haben. Zur Feststellung einer möglichen Atrophie dient die Ko-Registrierung, wobei Fusions- und Subtraktionstechniken insbesondere bei hoher T2-Läsionsdichte hilfreich sind.8 Als weiteres Hilfsmittel hat sich die optische Kohärenztomografie gut weiterentwickelt und wird diagnoseunterstützend und zukünftig auch in der Verlaufskontrolle eingesetzt werden.9
Biomarker für die Diagnostik und Verlaufsbeurteilung
Bei den Flüssigkeitsbiomarkern für die klinische MS-Beurteilung hat sich in den letzten Jahren viel getan. Eine initiale Liquoruntersuchung ist hier nicht nur wichtig, um eine chronische Immunaktivierung nachzuweisen, sondern unterstützt auch die Differenzialdiagnostik. So können unter anderem der IgG-Index oder die sensitiverenoligoklonalen Banden (OCB) bestimmt werden. Neu hinzugekommen ist der Index der Kappa-freien Leichtketten (k-FLC), der eine vergleichbare Sensitivität wie die Bestimmung der IgG-OCB erreicht, aber im Labor einfacher durchgeführt werden kann. Darüber hinaus berücksichtigt der Index der Kappa-freien Leichtketten neben IgG auch die Synthese von IgA- und IgM-Antikörpern, was ein umfassenderes Bild der intrathekalen Immunglobulinproduktion liefert.10,11
Neurofilamente und Gliamarker zur klinischen MS-Beurteilung
„Ein weiterer Biomarker, der eine immer zentralere Bedeutung erlangt, sind die Neurofilamente (NfL)“, erklärt Khalil. Diese werden bei neuroaxonaler Schädigung freigesetzt und können im Liquor und mit sensitiven Methoden, wie dem „single molecule array“ (SIMOA), auch im Blut nachgewiesen werden.12,13 Somit sind NfL-Werte krankheitsübergreifend verwendbar und gut für das Monitoring geeignet.14
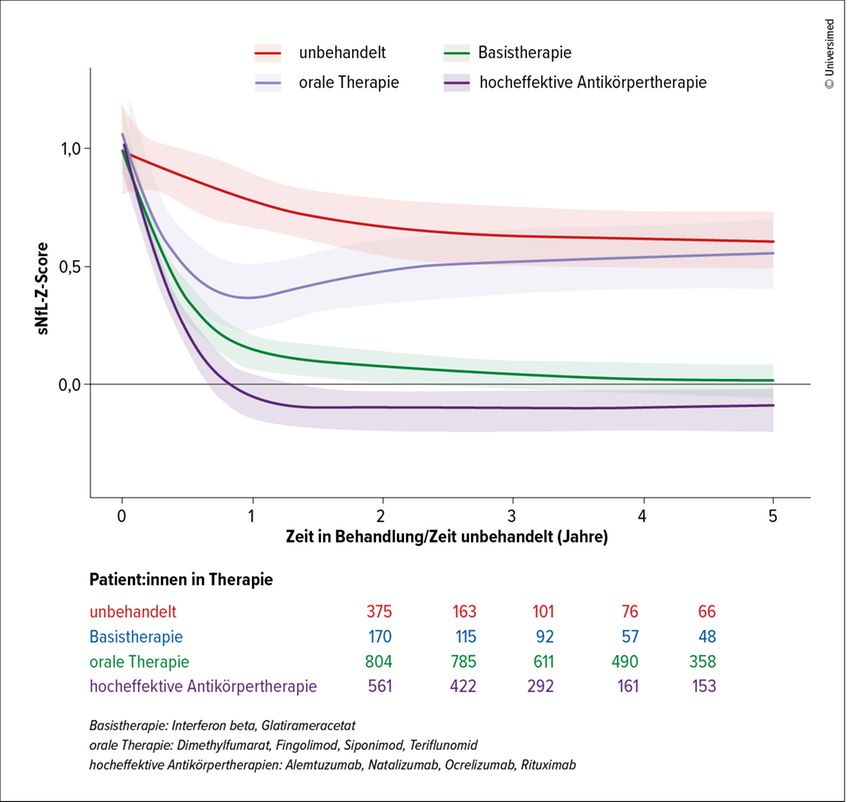
In einer rezenten Studie wurden Alters- und Body-Mass-Index(BMI)-korrigierte NfL-Z-Scores ermittelt, welche bisher die beste Annäherung für die Ermittlung individueller, klinisch anwendbarer NfL-Werte lieferten. Zudem konnte gezeigt werden, dass diese Z-Scores in der Tat auch Behandlungsverläufe abbilden (Abb. 1). Neben ihrer Aussagekraft zur Krankheitsaktivität konnte der Nutzen der NfL-Z-Scores auch bei der Krankheitsprädiktion über einen längeren Zeitraum gezeigt werden.15
Abb. 1: Zeitliche Entwicklung der Neurofilament-Z-Werte im MS-Krankheitsverlauf(modifiziert nach Benkert P et al.)15
Mit dem Gliamarker GFAP wird aktuell ein weiterer Blutbiomarker mit klinischer Anwendbarkeit erforscht. So konnte gezeigt werden, dass eine gemeinsame Erhöhung von NfL und GFAP ein Prädiktor für ein besonders hohes Risiko einer Krankheitsprogression ist.16,17 Die gängigen Methoden zur Entdeckung und Validierung biofluidbasierter Biomarker in der Neurologie wurden rezent zusammengefasst.18
Quelle:
22. Jahrestagung der Österreichischen Gesellschaft für Neurologie (ÖGN), Vorträge von Priv.-Doz. Dr. Harald Hegen und Assoz. Prof. Priv.-Doz. Dr. Michael Khalil, 12.–14. März 2025, Innsbruck
Literatur:
1 Hemmer B et al.: Deutsche Gesellschaft für Neurologie, Stand 12/2024 2 He A et al.: Timing of high-efficacy therapy for multiple sclerosis: a retrospective observational cohort study. Lancet Neurol 2020; 19(4): 307-16 3 Malpas CB et al.: Early clinical markers of aggressive multiplesclerosis. Brain 2020; 143(5): 1400-13 4 Tintore M et al.: The long-term outcomes of CIS patients in the Barcelona inception cohort: Looking back to recognize aggressive MS. Mult Scler 2020; 26(13): 1658-69 5 Olsson T et al.: Anti-JC virus antibody prevalence in a multinational multiple sclerosis cohort. Mult Scler 2013; 19(11): 1533-8 6 Rotstein D et al.: Reaching an evidence-based prognosis for personalized treatment of multiple sclerosis. Nat Rev Neurol 2019; 15(5): 287-300 7 Rocca MA et al.: Current and future role of MRI in the diagnosis and prognosis of multiple sclerosis. Lancet Reg Health Eur 2024; 44: 100978 8 Wattjes MP et al.: 2021 MAGNIMS-CMSC-NAIMS consensus recommendations on the use of MRI in patients with multiple sclerosis. Lancet Neurol 2021; 20(8): 653-70 9 Krämer J et al.: Evolution of retinal degeneration and prediction of disease activity in relapsing and progressive multiple sclerosis. Nat Commun 2024; 15(1): 5243 10 Di Filippo M et al.: Fluid biomarkers in multiple sclerosis: from current to future applications.Lancet Reg Health Eur 2024; 44: 101009 11 Hegen H et al.: Cerebrospinal fluid kappa free light chains for the diagnosis of multiple sclerosis: A systematic review and meta-analysis. Mult Scler 2023; 29(2): 169-81 12 Khalil M et al.: Neurofilaments as biomarkers in neurological disorders. Nat Rev Neurol 2018; 14(10): 577-89 13 Wilson DH et al.: The Simoa HD-1 analyzer: a novel fully automated digital immunoassay analyzer with single-molecule sensitivity and multiplexing. J Lab Autom 2016; 21(4): 533-47 14 Bridel C et al.: Diagnostic value of cerebrospinal fluid neurofilament light protein in neurology: a systematic review and meta-analysis. JAMA Neurol 2019; 76(9): 1035-48 15 Benkert P et al.: Serum neurofilament light chain for individual prognostication of disease activity in people with multiple sclerosis: a retrospective modelling and validation study. Lancet Neurol 2022; 21(3): 246-57 16 Abdelhak A et al.: Blood GFAP as an emerging biomarker in brain and spinal cord disorders. Nat Rev Neurol 2022; 18(3): 158-72 17 Meier S et al.: Serum glial fibrillary acidic protein compared with neurofilament light chain as a biomarker for disease progression in multiple sclerosis. JAMA Neurol 2023; 80(3): 287-97 18 Teunissen CE et al.: Methods to discover and validate biofluid-based biomarkers in neurodegenerative dementias. Mol Cell Proteomics 2023; 22(10): 100629
Das könnte Sie auch interessieren:
Auswahl von Erhaltungstherapien bei Myasthenia gravis
Durch eine Vielzahl an neuen biologischen Behandlungsalternativen konnte das Myasthenia-gravis-Therapiefeld weitreichend verbessert werden. Im Folgenden werden die Richtlinien zur ...
Interdisziplinäre Therapie der intrazerebralen Blutung
Aktuelle Studienergebnisse brachten erstmals einen positiven Effekt operativer Therapieverfahren auf das funktionelle Outcome bei Patient:innen mit intrazerebraler Blutung. Für die ...
Wenn das Sprechen schwerfällt – Dysarthrien verstehen und behandeln
Dysarthrien sind erworbene neurogene Störungen der Sprechmotorik, die die Ausführung und Koordination der für das Sprechen benötigten Bewegungen beeinträchtigen. Neben bekannten, ...