Der Weg von neoadjuvanter Therapie und radikaler Zystektomie hin zum Blasenerhalt
Autoren:
Dr. Sascha Mero
Dr. Kilian Gust
Abteilung für Urologie,
Medizinische Universität Wien
Comprehensive Cancer Center
E-Mail: sascha.mero@meduniwien.ac.at
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Beim diesjährigen Post EAU 2025 Meeting in Wien präsentierte Dr. Kilian Gust, FEBU (Medizinische Universität Wien), ein aktuelles Update zur systemischen Therapie des muskelinvasiven Urothelkarzinoms (MIBC). Im Mittelpunkt standen neue Evidenz zur perioperativen Immunchemotherapie sowie Entwicklungen in Richtung einer risikoadaptierten und organerhaltenden Behandlung.
Neoadjuvante und adjuvante Therapieoptionen
Die neoadjuvante Chemotherapie mit Gemcitabin/Cisplatin oder ddMVAC galt lange als Goldstandard bei Cisplatin-geeigneten Patient:innen mit MIBC. Für Patient:innen mit pathologischen Risikofaktoren nach radikaler Zystektomie (RC) (≥ypT2/ypN+ oder ≥pT3/pN+) hat sich die adjuvante Gabe von Nivolumab etabliert, gestützt auf die Ergebnisse der CheckMate-274-Studie.1 Die Auswahl der adjuvanten Therapie erfolgt zunehmend individualisiert und berücksichtigt neben dem pathologischen Tumorstadium auch die Cisplatin-Eignung, den PD-L1-Status sowie das Vorliegen einer neoadjuvanten Behandlung.
Bei Cisplatin-geeigneten Patient:innen, die vor der Operation eine neoadjuvante Chemotherapie erhalten haben, wird wie folgt differenziert:
-
D-L1-positiv: adjuvante Therapie mit Nivolumab
-
PD-L1-negativ: keine adjuvante Therapieoption, engmaschiges Follow-up
Für Cisplatin-geeignete Patient:innen, die keine neoadjuvante Therapie erhalten haben und bei denen nach Zystektomie ein hohes pathologisches Risiko vorliegt:
-
PD-L1-positiv: Nivolumab oder alternativ adjuvante Chemotherapie mit Gemcitabin/Cisplatin.
-
PD-L1-negativ: adjuvante Chemotherapie mit Gemcitabin/Cisplatin
Bei Cisplatin-ungeeigneten Patient:innen,typischerweise ohne neoadjuvante Therapie, richtet sich das Vorgehen ebenfalls nach dem PD-L1-Status:
-
PD-L1-positiv: adjuvantes Nivolumab, alternativ engmaschiges Follow-up
-
PD-L1-negativ: zumeist Follow-up, alternativ individuelle Entscheidung.
In prognostisch günstigen Situationen, z.B. bei pT2 pN0, ist die alleinige Nachsorge unabhängig vom PD-L1-Status in den meisten Fällen ausreichend.
Perioperative Immunchemotherapie
Die NIAGARA-Studie2 untersuchte erstmals ein vollständig perioperatives Therapiekonzept bei MIBC im kurativen Setting. Eingeschlossen wurden 1063 Patient:innen, davon 533 im experimentellen Arm (perioperativ Durvalumab) und 530 im Kontrollarm (postoperative Observation). Der experimentelle Arm umfasste eine neoadjuvante Kombination aus Gemcitabin und Cisplatin plus Durvalumab, gefolgt von RC und einer adjuvanten Immuntherapie mit Durvalumab über 12 Monate. Im Kontrollarm erhielten die Patient:innen eine neoadjuvante Chemotherapie mit Gemcitabin/Cisplatin, gefolgt von RC und anschließender Beobachtung.
Ein wesentlicher Vorteil dieses Studiendesigns ist die gezielte Berücksichtigung klinisch relevanter Subgruppen, die in früheren Studien häufig ausgeschlossen waren. Dazu zählen Patient:innen mit histologischen Varianten, cN1-Stadien sowie eingeschränkter Nierenfunktion (Kreatinin-Clearance 40–60ml/min), bei denen eine Cisplatin-basierte Therapie in gesplitteter Dosierung (Tag 1 und 8) ermöglicht wurde. Ein weiterer Vorteil ist die Unabhängigkeit vom PD-L1-Status, was die Anwendbarkeit in der klinischen Praxis erweitert. Primäre Endpunkte waren das ereignisfreie Überleben (EFS) und die pathologische Komplettremission (pCR), definiert als ypT0 ypN0 nach RC. Die präsentierten Daten zeigten eine pCR-Rate von 37,3%, ein Ergebnis im oberen Bereich bisheriger neoadjuvanter Strategien.
Zunehmend diskutiert wird der Stellenwert des pCR-Status als Entscheidungshilfe für oder gegen eine adjuvante Fortsetzung der Immuntherapie, wobei die Patient:innen im Rahmen der NIAGARA-Studie trotz pathologisch kompletten Ansprechensvon einer adjuvanten Gabe von Durvalumab profitierten. In der klinischen Praxis lehnt ein Teil der Patient:innen mit ypT0 nach RC eine Weiterbehandlung ab. Dabei bleibt zu berücksichtigen, dass der langfristige Therapieerfolg vermutlich wesentlich durch die adjuvante Sequenz beeinflusst wird.
Neue neoadjuvante Strategienund Blasenerhalt
Im Zuge der Entwicklung immunonkologischer Therapien gewinnt auch das Ziel des funktionellen Organerhalts zunehmend an Bedeutung. Bei selektierten Patient:innen mit kontrollierbarem Tumorverlauf kann eine RC vermieden oder verzögert werden – vorausgesetzt, dass die onkologische Sicherheit gewährleistet bleibt.
Ein aktueller Ansatz ist die Phase-II-Studie SunRISe-4,3 in der TAR-200, ein intravesikales Gemcitabin-Freisetzungssystem, mit dem PD-1-Inhibitor Cetrelimab kombiniert wird. Die präsentierten Daten zeigten eine pCR-Rate von 42% sowie eine objektive Ansprechrate von 62%, was das Potenzial lokal-systemischer Kombinationen für den Blasenerhalt unterstreicht.
Ein anderes Konzept verfolgt die CORE-002-Studie4 mit einem onkolytischen viralen Vektor (CG0070) in Kombination mit Nivolumab. Die intravesikale Applikation soll eine gezielte Tumorlyse mit lokaler Immunaktivierung bewirken. Erste Daten deuten auf eine immunvermittelte Wirksamkeit bei guter Verträglichkeit hin.
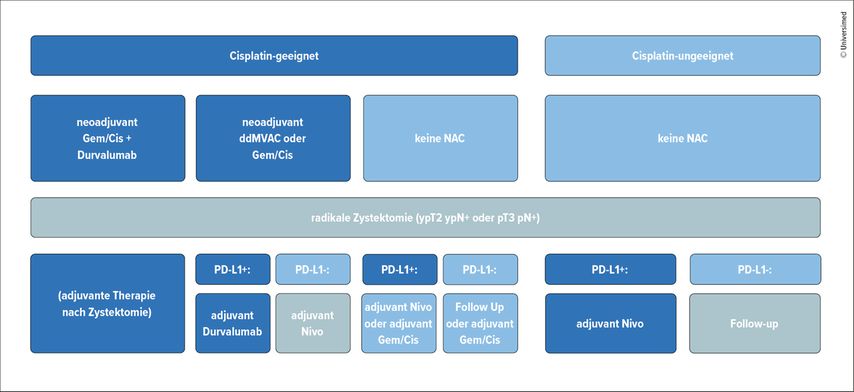
Abb. 1: Adjuvante Therapieoptionen nach Zystektomie bei MIBC in Abhängigkeit von NAC, Cisplatin-Eignung und PD-L1-Status (Vortrag von Dr. Kilian Gust, PostEAU 2025, Update Urothelkarzinom)
Für Cisplatin-ungeeignete Patient:innen befinden sich mehrere perioperative Strategien mit Enfortumab Vedotin in fortgeschrittener Prüfung. In der Phase-III-Studie EV-303/KEYNOTE-9055 wird die Kombination aus Enfortumab Vedotin und Pembrolizumab gegenüber RC allein un-tersucht. Die VOLGA-Studie6 evaluiert eine Dreifachkombination aus Enfortumab Vedotin, Durvalumab und Tremelimumab. Zu Patient:innen, die für eine Cisplatin-basierte neoadjuvante Chemotehrapie geeignet sind, erwarten wir in Kürze die Ergebnisse der EV-304/KEYNOTE-B15-Studie, welche die perioperative Gabe von Enfortumab Vedotin in Kombination mit Pembrolizumab im Vergleich zur neoadjuvanten Chemotherapie evaluiert.
All diese Studien zielen darauf ab, wirksamere, platinfreie Therapiealternativen zu etablieren, und schaffen aufgrund zu erwartender hoher Raten an pathologischerKomplettremissiongleichzeitig die Grundlage für einen potenziellen selektiven Blasenerhalt. Im Zuge dieser Entwicklungen rückt auch die Frage geeigneter Studienendpunkte in den Vordergrund. Klassische Parameter wie pCR oder EFS reichen nicht aus, um den klinischen Nutzen organerhaltender Konzepte vollständig zu erfassen. Ergänzend werden alternative Endpunkte wie „bladder-intact disease-free survival“, „complete clinical response“ und standardisierte Erhebungen der Lebensqualität (QoL) zunehmend relevant.
Parallel zur Weiterentwicklung der Therapiekonzepte gewinnt auch die Frage der adäquaten Verlaufskontrolle an Bedeutung. Neben Bildgebung wie CT, MRT, FDP-PET und Zystoskopie werden insbesondere zirkulierende Tumor-DNA (ctDNA) und urinbaiserte Tests (utDNA) als molekularer Marker intensiv untersucht. Ihr Einsatz könnte künftig helfen, minimale Resterkrankung frühzeitig zu erfassen und den adjuvanten Behandlungsbedarf präziser zu steuern.
Literatur:
1Aphase 3 randomized, double-blind, multi-center study of adjuvant nivolumab versus placebo in subjects with high risk invasive urothelial carcinoma (CheckMate 274: CHECKpoint Pathway and nivoluMAb Clinical Trial Evaluation 274). Online available: https://clinicaltrials.gov/study/NCT02632409 2 A phase III, randomized, open-label, multi-center, global study to determine the efficacy and safety of durvalumab in combination with gemcitabine + cisplatin for neoadjuvant treatment followed by durvalumab alone for adjuvant treatment in patients with muscle-invasive bladder cancer. Online available: https://clinicaltrials.gov/study/NCT03732677 3 A phase 2, open-label, multi-center, randomized study of tar-200 in combination with cetrelimab and cetrelimab alone in participants with muscle-invasive urothelial carcinoma of the bladder who are scheduled for radical cystectomy and are ineligible for or refusing platinum-based neoadjuvant chemotherapy. Online available: https://clinicaltrials.gov/study/NCT04919512 4 A phase 1 study of cg0070 combined with nivolumab in cisplatin ineligible patients with muscle invasive bladder cancer (MIBC). Online available: https://clinicaltrials.gov/study/NCT04610671 5A randomized phase 3 study evaluating cystectomy with perioperative pembrolizumab and cystectomy with perioperative enfortumab vedotin and pembrolizumab versus cystectomy alone in participants who are cisplatin-ineligible or decline cisplatin with muscle-invasive bladder cancer (KEYNOTE-905/EV-303) Online available: https://clinicaltrials.gov/study/NCT03924895 6 A phase IIIrandomized, open-label, multicenter study to determine the efficacy and safety of durvalumab in combination with tremelimumab and enfortumab vedotin or durvalumab in combination with enfortumab vedotin for perioperative treatment in patients ineligible for cisplatin or who refuse cisplatin undergoing radical cystectomy for muscle invasive bladder cancer (VOLGA). Online available: https://clinicaltrials.gov/study/NCT04960709
Das könnte Sie auch interessieren:
Highlights zum Prostatakarzinom vom EAU in Madrid
Zahlreiche im Rahmen des EAU-Kongresses 2025 in Madrid vorgestellte Arbeiten beschäftigten sich mit Diagnostik und Management des Prostatakarzinoms in allen Stadien der Erkrankung. So ...
Neue Entwicklungen im Management des benignen Prostatasyndroms
Die Therapie des benignen Prostatasyndroms (BPS) entwickelt sich hin zu individuell angepassten Strategien für jeden Patienten. Auf dem EAU-Kongress 2025 wurden Studien vorgestellt, die ...
Neues zur Li-ESWT in der Therapie der ED
Zwei Arbeiten zeigen den praktischen Einsatz der extrakorporalen Stoßwellentherapie mit niedriger Intensität (Li-ESWT; „low-intensity extracorporal shockwave therapy“) in der Therapie ...