Die neue Candida-Leitlinie 2025 in der klinischen Praxis
Bericht:
Reno Barth
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
2025 ist das Update der globalen Leitlinie zum Management von Candida-Infektionen erschienen. Die Guideline fasst die aktuelle Evidenz in Form übersichtlicher, praxisnaher Algorithmen zusammen. Dass das Befolgen dieser Empfehlungen das Outcome verbessert, wurde mittlerweile in einer internationalen Studie gezeigt.
Candidämie und invasive Candidiasisstellen weltweit ein infektiologisches Problem von erheblichem Ausmaß dar. Weltweit sind jährlich mehr als 600000 Menschen von Candidämie betroffen, was zu mehr als 250000 Todesfällen führt; an invasiver Candidiasis stirbt jährlich fast eine halbe Million Patient:innen.1
Als Risikofaktoren für eine Candidämie oder invasive Candidiasis nannte Univ.-Prof. Dr. Helmut Salzer, Leiter der Abteilung für Infektiologie und Tropenmedizin am Kepler Universitätsklinikum (KUK) in Linz, einen Aufenthalt auf der Intensivstation (5,5/1000 Aufnahmen, 37% Mortalität), invasive Zugänge, parenterale Ernährung, Langzeit-ICU-Behandlung, niedriges Geburtsgewicht (Neugeborene und Frühgeborene), Zustand nach chirurgischen Eingriffen, wobei insbesondere abdominelle Eingriffe (Anastomoseninsuffizienz) sowie rezidivierende Laparotomien problematisch sind. Ebenso erhöhen Langzeit- und/oder Breitspektrumantibiotika-Therapie das Risiko. Immunkompromittierte Patient:innen (Chemotherapie, SOT, HIV/AIDS, immunsuppressive Therapie, IL-17-Inhibitoren) weisen ebenso ein erhöhtes Risiko auf wie Hämodialyse- und/oder Patient:innen mit Diabetes oder akut nekrotisierender Pankreatitis.
Gemeinsame Guideline dreier Fachgesellschaften
Im Februar 2025 wurde von der European Confederation of Medical Mycology (ECMM) in Zusammenarbeit mit der International Society for Human and Animal Mycology (ISHAM) und der American Society for Microbiology (ASM) die aktuelle Leitlinie für das Management von Candida-Infektionen publiziert.
Die Global Guideline for the Diagnosis and Management of Candidiasis stellt einen umfassenden Review zu Diagnose, Behandlung und Prävention von Candida-Infektionen dar. Behandelt werden neben der Candidämie auch zahlreiche weitere klinische Problemstellungen wie zum Beispiel die Candida-Endokarditis, die okuläre Candidiasis, die ZNS-Candidiasis, Knochen- und Gelenksinfektionen oder die invasive Candidiasis bei Neugeborenen, Kindern und Jugendlichen. Die Empfehlungen werden in übersichtlichen Algorithmen für die einzelnen klinischen Situationen zusammengefasst.2
Dass es besser ist, diese Empfehlungen im klinischen Alltag auch anzuwenden, zeigt eine Studie, die an 64 Institutionen in 20 europäischen Ländern durchgeführt wurde.3 Die Arbeit kann auch als Hinweis auf die Gefährlichkeit von invasiven Pilzinfektionen gewertet werden, denn die 90-Tages-Mortalität lag bei 43%, wobei höheres Alter, ICU-Aufenthalt, höherer Charlson Comorbidity Index sowie Infektionen mit Candida tropicalis als Risikofaktoren gewertet wurden. Die Einhaltung der Leitlinien war mit einer höheren Überlebenswahrscheinlichkeit assoziiert, erläuterte Salzer, betonte jedoch auch, dass in das Dokument unterschiedliche Perspektiven eingeflossen sind und einzelne Empfehlungen daher einen gewissen Interpretationsspielraum offenlassen.
Ob und wie weit Leitlinien eingehalten werden, kann man mit dem EQUAL Candida Score bestimmen, der auf der Website der ECMM heruntergeladen werden kann.4 Der Score sammelt und wägt Faktoren ab, die zum idealen Umgang mit Candidämien empfohlen sind. Er liefert ein Werkzeug für das antimykotische Vorgehen sowie zur Bestimmung der Leitlinienadhärenz. Ein höherer EQUAL Candida Score bedeutet eine bessere Einhaltung der Leitlinien.5
Die Organbeteiligung bestimmt die Wahl und die Dauer der Therapie
Wie die Anwendung dieser Empfehlungen in der Praxis aussehen kann, demonstrierte Salzer am Beispiel eines 63-jährigen Patienten mit Alkoholabusus, chronischer Pankreatitis und chronischer Niereninsuffizienz sowie einer Whipple-OP und einer Chemotherapie bei Oropharynx-Ca in der Vorgeschichte. Der Patient war kachektisch und wurde über ein Port-a-Cath-System parenteral ernährt. Die Vorstellung erfolgte aufgrund einer akuten Visus-Verschlechterung. Eine endogene Endophthalmitis mit typischer Trübung des Glaskörpers und kleinen, weißen Läsionen wurde diagnostiziert, nach Glaskörperpunktion erfolgte der kulturelle Nachweis von C. albicans.
Der Patient wurde mit okulärer Candidiasis auf die Infektiologie verlegt, wo sowohl peripher als auch aus dem Port-a-Cath Blutkulturen abgenommen wurden. Die Kulturen waren positiv auf C. albicans und C. glabrata. Der Port-a-Cath wurde entfernt und es folgte die weitere Infektfokussuche. Dabei zeigten sich im Thorax-CT multiple pulmonale septische Absiedelungen als Hinweis auf eine Candida-Sepsis. Damit wurde die Diagnose einer Katheter-assoziierten Candidämie mit okulärer Candidiasis (C. albicans) und septisch pulmonalen Absiedelungen (C. albicans, C. glabrata) gestellt. Die Leitlinie empfiehlt bei Candida-Endophthalmitis als gleichberechtigte Optionen Fluconazol, liposomales Amphotericin B und Voriconazol. Alternativ könnte auf der Ophthalmologie auch Amphotericin B direkt in den Glaskörper eingebracht werden. Salzer wies darauf hin, dass sich unter den empfohlenen Substanzen kein Echinocandin findet, obwohl Echinocandine bei Candida-Infektionen erste Wahl sind. Die okuläre Candidiasis stellt diesbezüglich jedoch eine Ausnahme dar.
Da es sich im konkreten Fall jedoch um eine disseminierte Candidiasis handelt, muss das Vorgehen entsprechend angepasst werden. Bei der chronisch disseminierten Candidiasis empfiehlt die Leitlinie als First-Line-Optionen Caspofungin oder liposomales Amphotericin B. Caspofungin zählt zu den Echinocandinen, ist jedoch die einzige Substanz aus dieser Gruppe, für die Evidenz in dieser Indikation besteht. Dass andere Echinocandine ebenfalls wirksam wären, ist plausibel, aber nicht auf demselben Evidenzniveau gesichert.
Im konkreten Fall fiel die Wahl initial auf Voriconazol und Caspofungin. Der Patient entwickelte jedoch eine schwere Vigilanzminderung, die auf Voriconazol zurückgeführt wurde. Es erfolgte eine Umstellung auf Fluconazol und Caspofungin. Die Vigilanzminderung besserte sich nach Absetzen von Voriconazol.
In weiterer Folge entwickelte der Patient jedoch auch ausgeprägte Schmerzen im Bereich der Lendenwirbelsäule. Das MRT zeigte eine Spondylodiszitis TH11–TH12, die CT-gezielt punktiert wurde. In der Kulturwurde C. albicans nachgewiesen. Damit lag nun auch eine zusätzliche Knochenbeteiligung vor. Dies sei insofern von hoher Relevanz, als sich damit die empfohlene Therapiedauer deutlich verlängert. Die Leitlinie empfiehlt bei okulärer Candidiasis vier bis sechs Wochen, bei pulmonalen Abszessen mindestens sechs Monate, bei ossärer Candidiasis jedoch mindestens ein Jahr.
Vereinfachte Therapie und schnelles Ansprechen mit Rezafungin
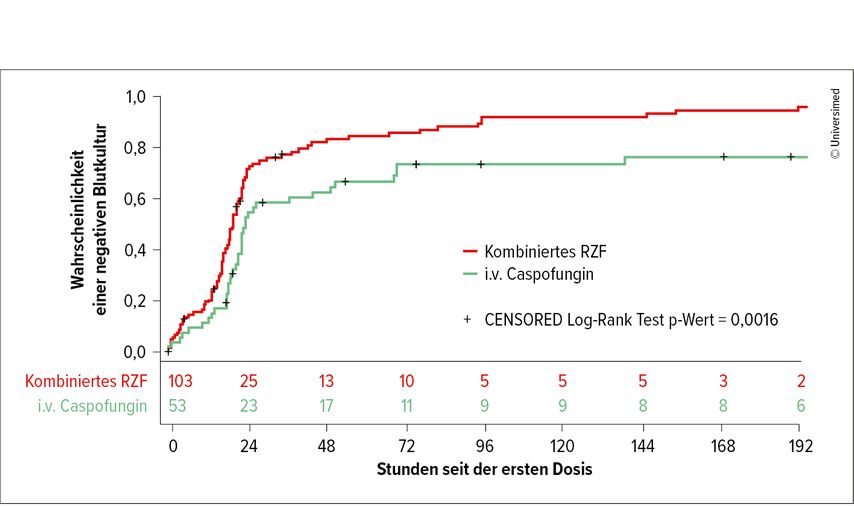
Zu den Risikofaktoren für eine Candidämie zählt auch der intravenöse Drogenabusus, wie Salzer am Fall eines 47-jährigen Patienten mit Spondylodiszitis mit spinalem Abszess schilderte. Der Patient war HIV- und HCV-positiv, die Anamnese ergab i.v. Drogenabusus. Die stationäre Aufnahme erfolgte aufgrund von Schmerzen in der Lendenwirbelsäule und Fieber. Im MRT wurde eine Spondylodiszitis mit spinalem Abszess gefunden, die Blutkultur ergab eine Infektion mit Candida dubliniensis. Wenn keine Organbeteiligungen vorliegen, ist die Wahl des Animykotikums wie in diesem Fall einfach, so Salzer. Starke Empfehlungen bestehen für die Echinocandine (Caspofungin, Anidulafungin, Micafungin und Rezafungin). Salzer wies darauf hin, dass mit Rezafungin aufgrund seiner längeren Halbwertszeit von 80–150 Stunden eine einmal wöchentliche Gabe möglich ist. Dies ist insofern relevant, als die tägliche Gabe von i.v. Echinocandinen bisher häufig zu verlängerten Krankenhausaufenthalten führte. Für Rezafungin sind auch keine Dosisanpassungen an Alter, Leber- oder Nierenfunktion erforderlich. Studiendaten zeigen ein rasches Ansprechen auf die Therapie (Abb. 1).6
Abb. 1: Zeit bis zur negativen Blutkultur nach Behandlung mit Rezafungin (RZF) im Vergleich zu i.v. Caspofungin (modifiziert nach Thompson GR et al. 2021)6
Tägliche Kontrollen des Therapieerfolgs
Der Therapieerfolg muss bei Candidämie durch regelmäßige Blutkulturen (z.B. alle 2 Tage) kontrolliert werden. Ist die Blutkultur am Tag 5 noch positiv, sollte das Vorgehen überprüft werden. Sollte eine Zweitlinientherapie erforderlich werden, bevorzugt die Leitlinie Amphotericin B aufgrund der besseren Verträglichkeit. Die Guideline empfiehlt bei Candidämie, alle Patient:innen auf Endokarditis und ZNS-Beteiligung (Abszesse, Meningitis) zu untersuchen. Auch an die Möglichkeit einer okulären Candidiasis muss gedacht werden. Ab der letzten positiven Blutkultur soll noch zwei Wochen therapiert werden.
Von entscheidender Bedeutung für die Wahl der Therapie bei Candidämie sind wie erwähnt eventuelle Organbeteiligungen, die Therapiedauer und Medikamentenwahl bestimmen. Die Methode der Wahl in der Detektion von Organbeteiligungen ist die Bildgebung, Salzer betonte jedoch auch die Bedeutung der klinischen Einschätzung („man muss den Patienten sehen“).
Der Erregernachweis erfolgt aus der Blutkultur, was allerdings nicht immer einfach ist, denn die Sensitivität liegt zwischen 21 und 71% und ist abhängig von der Art der Infektion, der abgenommenen Blutmenge pro Blutkulturflasche, einer etwaigen antifungalen Prophylaxe bzw. einer empirischen Therapie.7 Zusätzlich zur Kultur kann eine mikroskopische Abklärung erforderlich sein. Biomarker haben aktuell nur den Stellenwert eines Add-ons und ermöglichen alleine weder eine Diagnose noch ein Therapiemonitoring.
Quelle:
„ESC Candida Guideline – Praktikabel und hilfreich?“, Vortrag von Univ.-Prof. Dr. Helmut Salzer, Linz, am 21.3.2025 im Rahmen des ÖIK in Saalfelden
Literatur:
1 Denning DW: Lancet Infect Dis 2024; 24(7): e428-e438 2 Cornely OA et al.: Lancet Infect Dis 2025; 25(5): e280-93 3 Hoenigl M et al.: Lancet Infect Dis 2023; 23(6): 751-61 4 https://www.ecmm.info/equal-scores/ ; zuletzt aufgerufen am 23.10.2025 5 Mellinghoff SC et al.: Mycoses 2018; 61(5): 326-30 6 Thompson GR et al.: Clin Infect Dis 2021; 73(11): e3647-55 7 Kullberg BJ, Arendrup MC: N Engl J Med 2015; 373(15): 1445-56
Das könnte Sie auch interessieren:
Antimykotika-resistente Pilze sind in Österreich (noch) ein seltenes Problem
Ebenso wie Antibiotikaresistenzen werden auch Resistenzen von Pilzen gegen Antimykotika weltweit zum Problem – von dem Österreich glücklicherweise bislang kaum betroffen ist. ...
HIV-Infektion im Alter: Was sind die Herausforderungen?
Dank des medizinischen Fortschritts ist HIV heute eine chronische behandelbare Erkrankung mit nahezu normaler Lebenserwartung. Immer mehr HIV-positive Menschen erreichen ein höheres ...
Neue Möglichkeiten der Prävention durch Impfung
In den letzten Jahren wurden Impfstoffe gegen mehrere Erkrankungen auf den Markt gebracht, für die es bislang keine Möglichkeit der Impfprophylaxe gab. Das betrifft die Tropenkrankheiten ...